
告广大消费者
辽宁金丹药业有限公司(下称我司)成立于2002年1月25日,于2021年5月被康驰集团全资收购。此后,我司重启药品GMP符合性检查认证工作,具体如下:
2022年01月27日
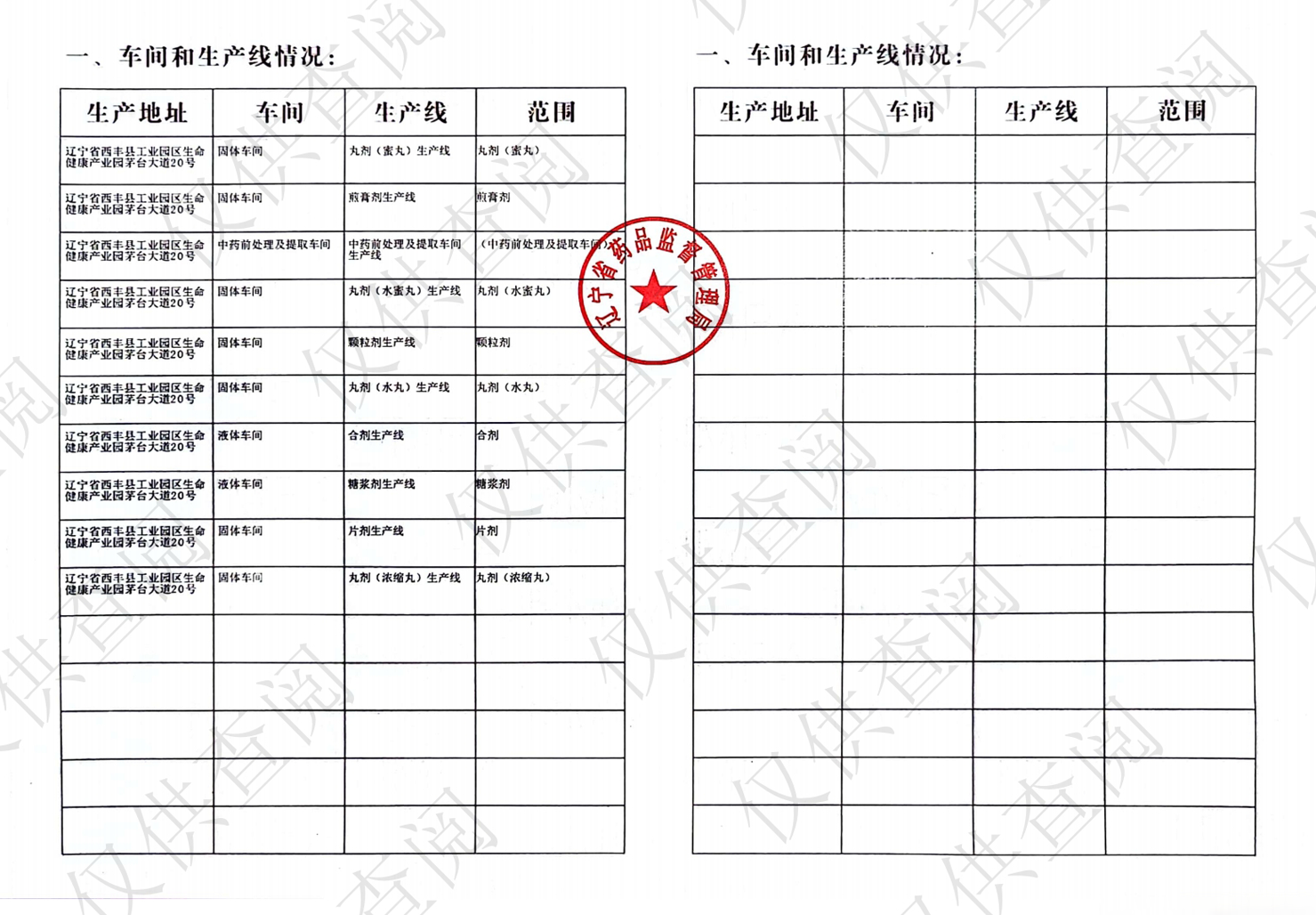
通过了丸剂(蜜丸)、煎膏剂、中药前处理及提取车间的药品GMP符合性现场检查,《药品GMP符合性现场检查结果通知书》编号为辽22010005;
2022年11月25日
通过了丸剂(水蜜丸)、颗粒剂的药品GMP符合性现场检查,《药品GMP符合性现场检查结果通知书》编号为辽22010041;
2022年12月21日
通过了合剂、丸剂(水丸)药品GMP符合性现场检查,《药品GMP符合性现场检查结果通知书》编号为辽22010044;
2023年11月06日
通过了片剂、糖浆剂、丸剂(浓缩丸)药品GMP符合性现场检查,《药品GMP符合性现场检查结果通知书》编号为辽23010049。
至此,我司所有剂型均通过了药品GMP符合性现场检查。
辽宁省药品监督管理局于2019年9月17日发布的“辽宁省药品监督管理局关于收回药品GMP证书的通知”辽药监(生)管[2019]91号和2020年7月1日发布的“辽宁省药品监督管理局关于注销《药品生产许可证》的公告”辽药监告[2020]27号均为我公司收购前企业行为,与我司重新获批药品GMP符合性检查认证之后的生产经营活动无关。
我司在重新获批药品生产资质的同时,对药品生产设备进行了升级改造,已具备现代化的生产能力。我司在生产药品过程中始终秉持“严把药品质量关,让百姓用放心药”的生产理念,对药品质量严格把控。未来,我司亦将严格遵照《药品管理法》《药品管理法实施条例》《药品生产监督管理办法》等相关法律法规组织生产,所生产的药品均系符合国家标准的合格药品。关于网络上流传的我司药品存在质量问题等负面信息多为不实信息,且均发生于我司被收购及重新获得《药品GMP符合性现场检查结果通知书》之前,与我司无关。

综上,我司出厂药品均为合格药品,请广大消费者放心购买并严格依据说明书或遵医嘱使用。
特此通告。
辽宁金丹药业有限公司
2024年03月15日